FDA’nın 23 Nisan 2026 tarihli açıklamasına göre Otarmeni, “lunsotogene parvec-cwha” adlı, çift adeno-associated virus yani çift AAV vektör temelli ilk gen tedavisi oldu. Tedavi, moleküler olarak doğrulanmış iki taraflı OTOF gen varyantı bulunan ve 90 dB HL’nin üzerinde işitme kaybı yaşayan hastalar için endike kabul edildi.
Bu onayı dikkat çekici kılan yalnızca tedavinin niteliği değil, değerlendirme süresinin hızı da oldu. FDA, bu başvurunun BLA dosyalamasından yalnızca 61 gün sonra onaylandığını, bunun Komiserin Ulusal Öncelik Kuponu pilot programı kapsamındaki altıncı onay ve bu program altındaki ilk gen tedavisi olduğunu duyurdu. Kuruma göre bu süreç, modern FDA tarihinde en hızlı biyolojik lisans onaylarından biriyle de eşdeğer konuma yerleşti.
OTOF genine bağlı sağırlıkta bugüne kadar hastalığın seyrini değiştiren bir tedavi seçeneği bulunmuyordu. FDA, bu gen kusurunun doğuştan işitme kaybı vakalarının önemli bir bölümünde rol oynadığını, iki işlevsiz OTOF kopyasına sahip hastalarda otoferlin üretilemediği için ses sinyallerinin düzgün iletilemediğini belirtti. Kurum, tanının gecikmesinin konuşma ve dil gelişiminde kalıcı kayıplara yol açabileceğine de dikkat çekti.
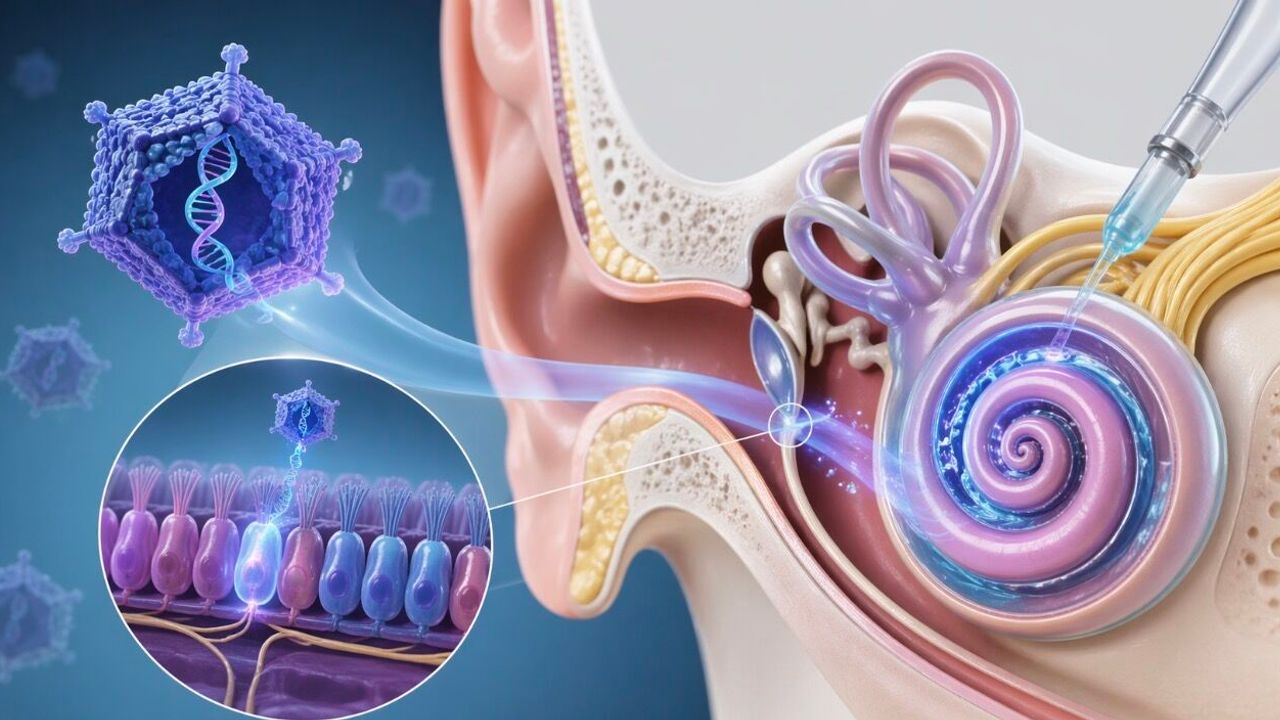
Tedavi tek dozluk bir biyolojik ürün ve cihaz kombinasyonu olarak uygulanıyor. FDA açıklamasına göre Otarmeni, cerrahi yolla kokleaya veriliyor; uygulamada enjektör, kateter ve infüzyon pompasından oluşan özel bir set kullanılıyor. Amaç, iç kulaktaki saç hücrelerine işlevsel OTOF genini ulaştırarak otoferlin üretimini ve işitsel sinyal iletimini yeniden başlatmak.
Onayın dayanağını ise halen süren çok merkezli, tek kollu bir klinik çalışma oluşturdu. Çalışmada 10 aylık ile 16 yaş arasındaki 24 çocuk hasta değerlendirildi. FDA, etkinlik açısından değerlendirilebilen 20 hastanın yüzde 80’inde işitmede iyileşme görüldüğünü, bunun hastalığın doğal seyrinde beklenen bir sonuç olmadığını bildirdi.
Bununla birlikte tedavi tamamen risksiz değil. Kurumun verdiği bilgiye göre en sık görülen yan etkiler orta kulak enfeksiyonu, bulantı, baş dönmesi ve işlem kaynaklı ağrı oldu. Ayrıca cerrahi komplikasyonlar açısından dikkatli izlem önerildi. İç kulağa güvenli erişimi engelleyen anatomik sorunları olan hastalarda ise bu tedavinin önerilmediği belirtildi.
FDA, Otarmeni başvurusuna yetim ilaç, nadir pediatrik hastalık, fast track ve RMAT statüleri verildiğini açıkladı. Ürünün hızlandırılmış onay aldığı, kalıcı etkinlik ve özellikle konuşma gelişimi ile yaşam kalitesi üzerindeki etkilerin sonraki verilerle doğrulanmasının gerekeceği de vurgulandı. Bu ayrıntı, tedavinin umut verici sonuçlar verdiğini ancak uzun dönem izlemin hâlâ kritik olduğunu gösteriyor.
Gen tedavileri bugüne kadar daha çok nadir nörolojik ya da hematolojik hastalıklar üzerinden gündeme gelmişti. Bu onay ise işitme kaybı alanında ilk kez doğrudan genetik kusuru hedef alan bir yaklaşımın resmi olarak klinik kullanıma girdiğini gösteriyor. Özellikle erken tanı konan çocuklarda, yalnızca işitmenin değil konuşma ve sosyal gelişimin de geleceğini etkileyebilecek bir başlık açılmış oldu. Bu çıkarım, FDA’nın erken tanı ve gecikmiş tedavi penceresine ilişkin değerlendirmesiyle uyumlu görünüyor.
Kısacası FDA’nın Otarmeni kararı, sağırlık tedavisinde yalnızca yeni bir ilaç onayı değil, yeni bir tedavi mantığının da kabulü anlamına geliyor. Klinik izlemler ve uzun dönem sonuçlar yakından takip edilecek olsa da, genetik işitme kaybı yaşayan hastalar için bu gelişme şimdiden tıp tarihinde ayrı bir başlık açmış durumda.