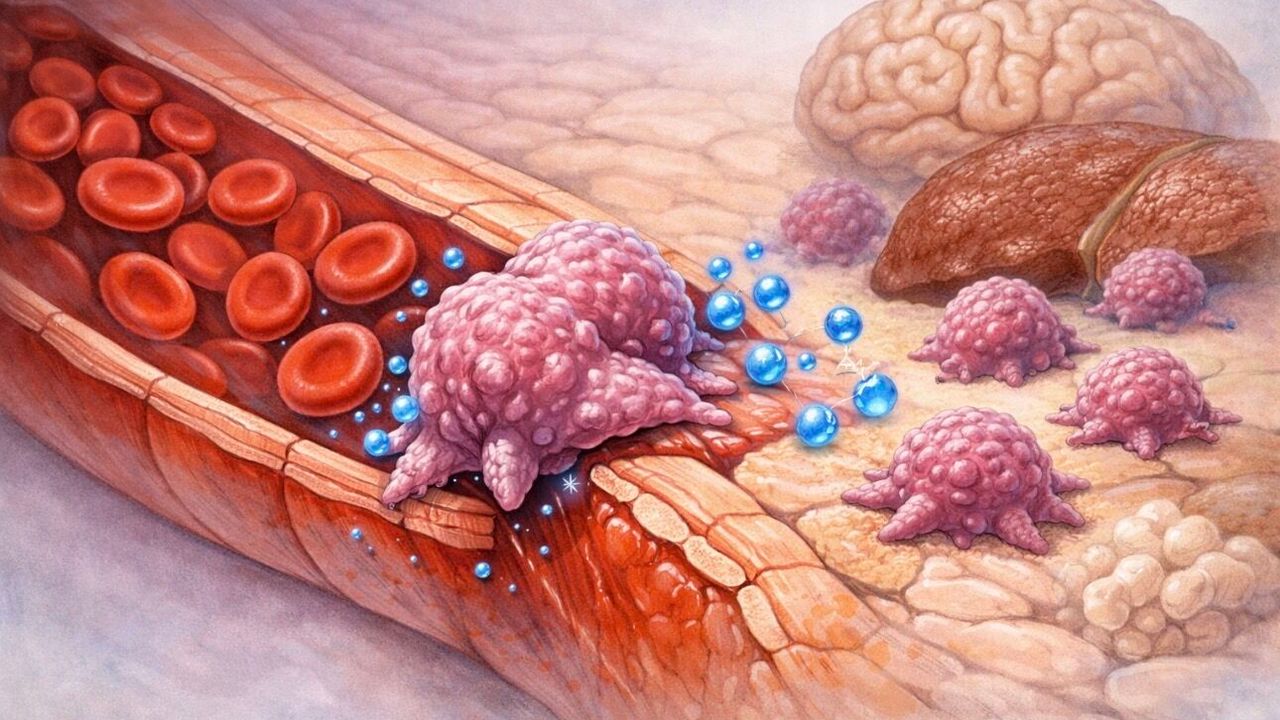
Kanser hastalarında en ağır tabloyu çoğu zaman birincil tümör değil, tümörün başka organlara yayılması oluşturuyor. Akciğer kanserinin beyne ya da karaciğere, mide kanserinin peritona yayılması gibi metastatik süreçler, tedavi seçeneklerini daraltan en kritik aşamalar arasında yer alıyor. İşte bu ölümcül zincirin en önemli halkalarından biri olan “damar dışına çıkış” sürecine ilişkin dikkat çekici bir bulgu Japonya’dan geldi. Kyushu Üniversitesi araştırma ekibi, kanser hücrelerinin damar duvarını aşarak yeni dokulara yerleşmesinde kullanılan temel hareket mekanizmasının, embriyonik gelişimde görev alan hücrelerin kullandığı bir programla şaşırtıcı ölçüde benzer olduğunu ortaya koydu. Çalışma, Nature Communications’ta 26 Mart 2026’da yayımlandı.
Araştırmanın merkezinde, hücre zarında geçici kabarmalar oluşturan “bleb” adı verilen yapılar bulunuyor. Ekip, kuş embriyolarındaki primer germ hücrelerini ve farklı insan kanser hücrelerini inceleyerek, her iki hücre tipinin de damar dışına çıkarken bu zar çıkıntılarından yararlandığını gösterdi. Başka bir ifadeyle, ileride sperm ya da yumurta hücresine dönüşecek gelişimsel hücrelerle metastatik kanser hücreleri, biyolojik amaçları tamamen farklı olsa da, damar duvarını aşmak için benzer bir fiziksel hareket düzeni kullanıyor.
Bilim insanlarına göre asıl çarpıcı nokta, bu ortaklığın yalnızca yüzeysel bir benzerlik olmaması. Çalışma, “kanser metastazı tamamen rastgele ortaya çıkan bir hücresel sapma mı?” sorusuna yeni bir pencere açıyor. Bulgular, kanser hücrelerinin, organizmanın çok erken gelişim evrelerinde kullanılan eski ve temel bir hücre hareket programını yeniden devreye sokuyor olabileceğine işaret ediyor. Bu bakış, metastazı sadece saldırgan bir bozulma olarak değil, bedenin kendi biyolojik yazılımının kötüye kullanılması olarak da okumaya imkân tanıyor. Bu yorum, çalışmanın verilerinden çıkarılan bilimsel bir çerçeve niteliğinde.
Araştırma aynı zamanda tedavi açısından kritik bir ayrımı da ortaya koydu. Her iki hücre tipi de bleb kullansa da, bu yapıyı tetikleyen kalsiyum sinyali aynı değil. Kyushu Üniversitesi’nin açıklamasına göre primer germ hücrelerinde bleb oluşumu, hücre içi depolardan kalsiyum salan IP3 reseptörü üzerinden düzenlenirken; kanser hücrelerinde süreç daha çok hücre dışından kalsiyum girişine dayanan SOCE mekanizmasına bağlı görünüyor. Yani araç ortak, ama kontak anahtarı farklı.
Bu ayrımın önemi büyük. Çünkü metastazı durdurmaya yönelik gelecekteki ilaç stratejileri, teorik olarak kanser hücrelerinin kullandığı kalsiyum devresini hedef alıp normal gelişimsel hücre işlevlerini daha az etkileyebilir. Üniversitenin değerlendirmesinde de bu bulgunun, metastazı baskılamaya dönük yeni tedavi stratejilerine kapı aralayabileceği, ancak şimdilik bunun temel bilim düzeyinde bir keşif olduğu vurgulanıyor. Yani henüz “metastazı durduran ilaç bulundu” demek için erken; fakat metastazın en kritik evrelerinden birine ait mekanik haritanın daha net çizildiği söylenebilir.
Çalışmanın yazarları arasında Mizuki Morita, Manami Morimoto, Junichi Ikenouchi, Bertrand Pain, Yuji Atsuta, Yoshiki Hayashi, Takayuki Teramoto ve Daisuke Saito yer alıyor. Araştırma, Kyushu Üniversitesi ile Fransa’daki INSERM bağlantılı iş birliklerini de içeren disiplinlerarası bir zeminde yürütüldü. Bu yönüyle çalışma, gelişim biyolojisi ile kanser biyolojisini aynı masada buluşturarak metastaz araştırmalarında yeni bir kavramsal hat çiziyor.