Özellikle bazı kan kanserlerinde çarpıcı sonuçlar veren bu yöntem, klasik kemoterapi ve radyoterapiden farklı olarak doğrudan bağışıklık sistemini hedef alıyor. ABD Ulusal Kanser Enstitüsü’ne göre CAR-T tedavisinde hastadan alınan T hücreleri genetik olarak değiştirilerek kanser hücrelerini tanıyıp yok edecek hale getiriliyor ve ardından yeniden hastaya veriliyor.
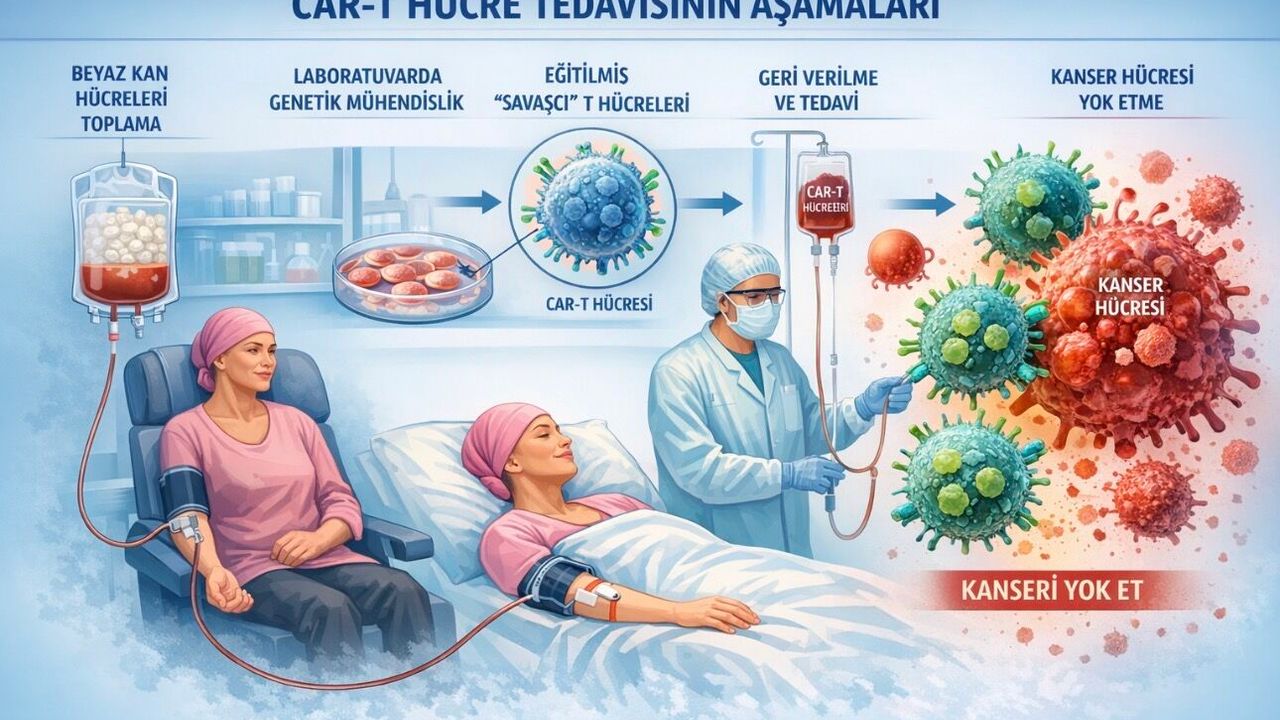
CAR-T’nin açılımı “Chimeric Antigen Receptor T-cell” yani “Kimerik Antijen Reseptörü Taşıyan T Hücresi” anlamına geliyor. Basit ifadeyle bu tedavi, vücudun doğal savunma askerleri olan T hücrelerine yeni bir hedefleme sistemi yüklenmesi demek. Böylece bağışıklık hücreleri, kanser hücrelerini daha net tanıyabiliyor ve onlara karşı daha güçlü bir saldırı başlatabiliyor. NHS İngiltere, bu yöntemin her hasta için özel üretildiğini ve bu yönüyle standart ilaç tedavilerinden ayrıldığını vurguluyor.
Tedavi süreci ise birkaç aşamadan oluşuyor. Önce hastadan beyaz kan hücreleri toplanıyor. Daha sonra bu hücreler laboratuvarda genetik olarak değiştiriliyor, çoğaltılıyor ve uygun hazırlık sürecinin ardından tekrar hastaya veriliyor. Bu yönüyle CAR-T, “hazır ilaç”tan çok, adeta kişiye özel üretilmiş canlı bir tedavi olarak tanımlanıyor. ABD Ulusal Kanser Enstitüsü, bu yaklaşımın özellikle daha önce tedavi görmüş ama hastalığı tekrarlamış bazı hastalarda umut verici sonuçlar sunduğunu belirtiyor.
Bugün için CAR-T tedavisi en çok lösemi, lenfoma ve multiple myelom gibi bazı hematolojik kanserlerde öne çıkıyor. Mayo Clinic ve Cancer Research UK’ye göre bu yöntem özellikle belirli B hücreli lösemi ve lenfoma türlerinde, ayrıca bazı multipl miyelom olgularında kullanılabiliyor. ABD Gıda ve İlaç Dairesi’nin güncel listesinde CAR-T sınıfında birden fazla onaylı ürün bulunuyor ve bu alan genişlemeye devam ediyor. Aralık 2025’te FDA, Breyanzi için marjinal zon lenfomada yeni bir kullanım onayı da verdi.
Ancak bu tedavi bir mucize manşetinden ibaret değil. Uzmanlar, CAR-T’nin güçlü olduğu kadar ciddi yan etkiler de taşıyabildiğine dikkat çekiyor. En çok izlenen riskler arasında sitokin salınım sendromu (CRS) ve nörolojik toksisite yer alıyor. NCI, bu nörolojik tablonun “ICANS” olarak adlandırıldığını belirtirken, Amerikan Kanser Derneği de enfeksiyonlar, düşük kan hücresi sayımları ve bağışıklık sisteminin baskılanması gibi başka ciddi sorunların görülebileceğini aktarıyor.
FDA da güvenlik başlığını yakından izliyor. Kurum, 2025 yılında bazı CAR-T ürünlerinde REMS zorunluluğunu kaldırsa da bunun nedeni risklerin ortadan kalkması değil, bu yan etkilerin yönetiminde klinik deneyimin artmış olması. FDA, ürün etiketlerinde sitokin salınım sendromu ve nörolojik toksisite için kutulu uyarıların sürdüğünü açıkça belirtiyor. Ayrıca 2024’te bazı CAR-T tedavileri için ikincil T-hücre malignitesi riskine ilişkin kutulu uyarı da duyuruldu.
Bilim dünyasının asıl büyük hedefi ise CAR-T’yi yalnızca kan kanserleriyle sınırlı bırakmamak. 2025 tarihli bilimsel derlemelerde, CAR-T’nin solid tümörlerde de etkili hale getirilmesi için yoğun çalışmalar yürütüldüğü, ancak tümör mikroçevresi, hedef seçimi ve güvenlik gibi önemli engellerin henüz tam aşılmadığı belirtiliyor. Yani teknoloji büyüyor, fakat önünde hâlâ zorlu bir biyolojik labirent var.
Sonuç olarak CAR-T, kanser tedavisinde ezber bozan bir yaklaşım olarak görülüyor. Hastanın kendi hücresinden üretilen bu tedavi, tıbbın artık yalnızca hastalığı değil, bağışıklık sisteminin dilini de yeniden yazmaya başladığını gösteriyor. Yine de uzmanlara göre bu yöntem, her hasta için uygun bir seçenek değil; yüksek teknoloji, dikkatli hasta seçimi ve deneyimli merkezler gerektiriyor. Umut büyük, fakat tedavi alanı hâlâ temkinli ilerleyen, pahalı ve karmaşık bir cephe olarak önemini koruyor.